水の分析は、その開始以来、近赤外分光法の分野に存在していました(Hirschfeld 1985、Grant、Davies、およびBilverstone 1989、Iwamoto、Uozumi、およびNishinari 1987、Maeda et al.1995)。これらの初期の研究は、水スペクトルの特性を分析して利用しましたが、分子システムおよび生物学的マトリックスとしての水の概念はまだ考慮されていませんでした。水は、その支配的な吸収のために、赤外線および近赤外線分光法の「最大の敵」とよく言われています。この態度には2つの理由があります。長い間、生物科学では水は不活性媒体と見なされていました。生きているプロセスは、遺伝子、DNA、タンパク質、代謝物、または他の単一の生体分子の観点から説明されました。当然のことながら、研究手法はこれらの生体分子の構造に関連した信号を抽出することに焦点を合わせており、近赤外領域では、水の支配的な吸光度がそれらの吸収帯を観察するための障害と見なされていました。しかし、水科学の分野は過去数十年で大きな進歩を遂げ、水に関する一般的な見解と生物システムにおけるその役割を大きく変えました(Pollack、Cameron、およびWheatley 2006、Del Giudice、Spinetti、およびTedeschi 2010、Ball 2008b、a、Chaplin 2006)。現在、水は活性溶媒として認識されており、その構造を溶質に適応させて適応させます。生物学的システムでは、生体分子および細胞プロセスのダイナミクスにおいて積極的な役割を果たす一種の生体分子です(Ball 2008a、Tsenkova 2008、 2009、2010)。
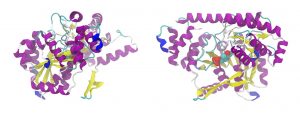
さまざまな生体分子と水との相互作用についての多方面にわたるアクアフォトミクスの研究を通じて、それらのダイナミクスとそこで水が果たす重要な役割についての見識を得ました。この分野で最初に応用されたものの1つは、プリオンタンパク質異性体の同定に関するものでした(Tsenkova et al.2004)。 銅(Cu)の代わりにマンガン(Mn)が結合することが、プリオンタンパク質を機能不全の形に変換するメカニズムの1つであると考えられています。水溶液中のMnおよびCu結合異性体のアクアフォトミクス分析により、、Mnの結合は不安定化と線維化の促進を引き起こすのに対して、Cuの結合は水中のタンパク質の安定性を高めることが明らかになりました。別の研究では、アミロイド線維の形成について研究されました(Chatani et al.2014)。並行して行われた研究により、2050〜2350 nmおよび1300〜1600nmのスペクトル領域でインスリンの小繊維化にともなう変化が観察されました。この結果により、タンパク質の形態変化プロセス全体が水分子集合形態(マトリックス)の変化に反映されることが示されました(Chatani et al.2014)。
Ball, P. 2008a. “Water as a biomolecule.” ChemPhysChem 9 (18):2677-2685.
Ball, P. 2008b. “Water as an active constituent in cell biology.” Chemical reviews 108 (1):74-108.
Chaplin, M. 2006. “Do we underestimate the importance of water in cell biology?” Nature Reviews Molecular Cell Biology 7 (11):861-866.
Chatani, E., Y. Tsuchisaka, Y. Masuda, and R. Tsenkova. 2014. “Water molecular system dynamics associated with amyloidogenic nucleation as revealed by real time near infrared spectroscopy and aquaphotomics.” PloS one 9 (7):e101997.
Del Giudice, E., P.R. Spinetti, and A. Tedeschi. 2010. “Water dynamics at the root of metamorphosis in living organisms.” Water 2 (3):566-586.
Grant, A., A.M.C. Davies, and T. Bilverstone. 1989. “Simultaneous determination of sodium hydroxide, sodium carbonate and sodium chloride concentrations in aqueous solutions by near-infrared spectrometry.” Analyst 114 (7):819-822.
Hirschfeld, Tomas. 1985. “Salinity determination using NIRA.” Applied spectroscopy 39 (4):740-741. doi: 10.1366/0003702854250293.
Iwamoto, M., J. Uozumi, and K. Nishinari. 1987. “Preliminary investigation of the state of water in foods by near infrared spectroscopy.” Proceedings of the International NIR/NIT Conference, Budapest, Hungary.
Maeda, H., Y. Ozaki, M. Tanaka, N. Hayashi, and T. Kojima. 1995. “Near infrared spectroscopy and chemometrics studies of temperature-dependent spectral variations of water: relationship between spectral changes and hydrogen bonds.” Journal of Near Infrared Spectroscopy 3 (4):191-201. doi: 10.1255/jnirs.69.
Pollack, G.H., I.L. Cameron, and D.N. Wheatley, eds. 2006. Water and the cell. Dordrecht, Netherlands: Springer.
Tsenkova, R. 2008. “Aquaphotomics: acquiring spectra of various biological fluids of the same organism reveals the importance of water matrix absorbance coordinates and the aquaphotome for understanding biological phenomena.” NIR news 19 (1):13-15.
Tsenkova, R. 2009. “Aquaphotomics: dynamic spectroscopy of aqueous and biological systems describes peculiarities of water.” Journal of Near Infrared Spectroscopy 17 (6):303-313. doi: 10.1255/jnirs.869.
Tsenkova, R. 2010. “Aquaphotomics: water in the biological and aqueous world scrutinised with invisible light.” Spectroscopy Europe 22 (6):6-10.
Tsenkova, R.N., I.K. Iordanova, K. Toyoda, and D.R. Brown. 2004. “Prion protein fate governed by metal binding.” Biochemical and biophysical research communications 325 (3):1005-1012. doi: 10.1016/j.bbrc.2004.10.135.